1.1 NVP及其聚合物
PVP是具有优异性能、用途广泛的一种非离子型水溶性高分子精细化学品,它是由NVP在一定的条件下聚合而成的,是N-乙烯基酰胺类官能团聚合物中最具特色,且被研究得最深入、广泛的精细化学品。自1938年德国乙炔化学家Reppe首次公开用乙炔为原料合成NVP及其聚合物PVP的专利[1]至今已经有六十多年的研究、生产和应用的历史,到目前已发展成为非离子、阳离子、阴离子三大类,工业级、医药级、食品级三种规格,共十几个品种,分子量从数千到一百万以上的均聚物、共聚物和交联聚合物系列产品,并以其优异独特的性能广泛应用于工农业生产和人民生活以及相关的科研部门,并仍以每年发表数百篇的文献展示其方兴未艾的现状和继续发展的前景。
1.1.1 NVP的性质
1.物理性质
NVP常温下是一种无色或者淡黄色、略有气味的透明液体,易溶于水,其主要的物理性质如下:
密度: 1.04(25℃)
熔点: 13.5℃
沸点: 148℃(13332.24Pa),58~65℃(13.3~26.64Pa)
闪点: 98.33℃
折光率:
NVP具有优良的溶液特性,除易溶于水外,还易溶于许多有机溶剂,如甲醇、乙醇、丙醇、异丙醇、三氯甲烷、甘油、四氢呋喃、乙酸乙烯酯等,还能溶于甲苯等芳香类溶剂。
一般说来,NVP在较强极性的溶剂中有比较好的溶解性,而在非极性溶剂中的溶解性较差,如表1.1所示。
表1.1 NVP在各种溶剂中的溶解性
溶剂 | 水 | 乙醇 | 苯 | 甲苯 | 丙酮 | 氯仿 | 1,4-二氧六环 |
溶解性 | √ | √ | √ | × | × | √ | × |
溶剂 | DMF | THF | 二甲苯 | 正戊醇 | 环己烷 | 乙酸乙酯 | 丙烯酸丁酯 |
溶解性 | √ | × | × | × | × | × | × |
溶剂 | 甲醇 | 丙醇 | 环己酮 | 戊烷 | 甲酸 | 二氯甲烷 | 甲基环己烷 |
溶解性 | √ | √ | × | × | √ | √ | × |
溶剂 | 乙酸 | 丙酸 | 石油醚 | 松节油 | 氯苯 | 四氯化碳 | 乙基乙烯基醚 |
溶解性 | √ | √ | × | × | × | × | × |
注: “√”表示可溶;“×”表示溶解性不好。
2.化学性质
NVP分子式为C6H9NO,结构为:
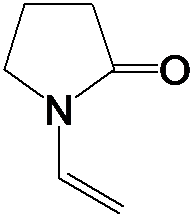
NVP的分子是一个含有N原子的五元环,属于内酰胺类化合物,在N原子上连有一个乙烯基,NVP这种特殊的分子结构赋予了它一些特殊的化学性质,其中最重要的就是易聚合性和易水解性。
NVP在适当的引发剂作用下,或者光照下即可发生聚合反应得到PVP,反应式如下:
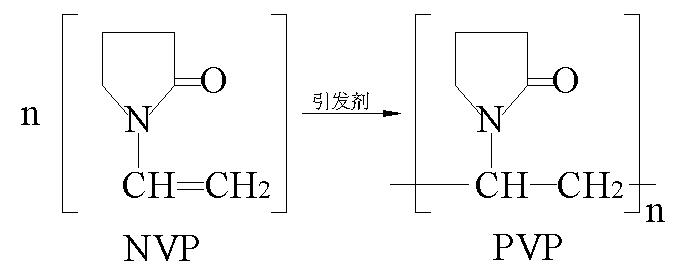
即使在没有引发剂的情况下,NVP放置的时间过长或者在运输过程中由于震动也可能发生不同程度的自聚合而影响其质量,所以市售的商品NVP中一般都加有阻聚剂,使用时可以用减压蒸馏或活性炭吸附的方法除去阻聚剂。
NVP的另一个重要的化学性质是在酸性或碱金属离子存在的条件下很容易发生水解反应,生成吡咯烷酮和乙醛,其水解过程如图1.1所示[2]。
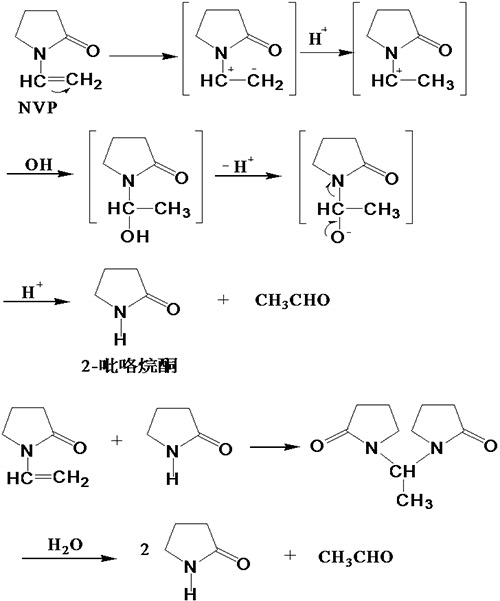
图1.1 NVP的水解
由于NVP易水解,所以在NVP的生产和使用中应注意两点:一是合成NVP时必须注意把水去除完全,保证产品中不含水分;二是在贮存、运输过程中,要使产品呈中性或弱碱性,从而防止水解与自聚合反应发生,通常的方法是加人0.1%的碱(如氢氧化钠、氨或低分子量的胺类)。
1.1.2 NVP的合成
PVP的聚合单体NVP,是1938年德国BASF公司化学家W. Reppe首次合成得到的[1]。他是以乙炔为起始原料,经过一系列化学反应,最后得到NVP。该合成方法被称为乙炔法,也叫Reppe法。
该方法是以乙炔、甲醛为起始原料,经过乙炔的醛加成、催化加氢、催化脱氢成环、氨解、炔加成等五步反应,最后得到NVP。其原理可用如图1.2的反应式表示[1,3-6]:
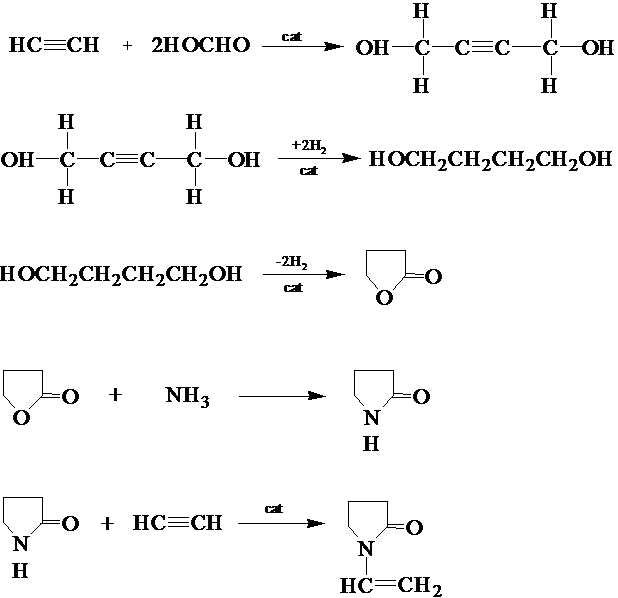
图1.2 NVP的乙炔法合成路线
乙炔法生产NVP工艺已相当成熟,是当今世界上工业生产NVP的主要方法之一。该工艺的主要优点是工艺成熟、原料便宜易得等,主要的不足之处是工艺流程长、固定资本投资大、操作条件要求严格,主要的原料乙炔存在爆炸危险性等。
近几十年来科技工作者在完善乙炔法的同时。也研究开发了或正在努力开发其他的NVP合成及生产方法。经过几十年发展,又出现了γ-丁内酯法、吡咯烷酮法、顺丁烯二酸酐法、琥珀酸法等多种合成NVP的方法[7-13]。但这些方法都处在进一步的研究中,有待于取得进一步的突破。
1.1.3 NVP的聚合反应
NVP单体在工业上并没有实际应用价值,只有将NVP聚合或共聚为具有一定结构、一定组成和一定分子量的高分子化合物之后,才能在工业上应用。
NVP可以均聚,也可以与其他单体共聚;得到的聚合物可以是线性的,也可以是交联聚合物。
1.均聚
NVP单体极容易发生聚合反应。把NVP单体加热到140℃以上,或者在NVP单体中加人引发剂很容易引发NVP的均聚,生成聚乙烯吡咯烷酮(PVP)。引发剂包括阳离子型引发剂,如BF3[14-15];阴离子型引发剂,如酰胺的钾盐;自由基引发剂,如过氧化物、偶氮类化合物等。与其他高分子的合成方法相似,NVP的聚合方式也有本体聚合、溶液聚合和悬浮聚合等几种。
本体聚合由于聚合过程中反应体系的粘度逐渐增大,聚合物扩散困难,反应热不容易移走,局部过热等原因,得到的产品质量不好,不能满足商业产品的要求,在工业生产上没有实际应用价值。悬浮聚合也少见报道。目前工业上NVP的聚合一般都是采用溶液聚合的方法,用于其溶液聚合的溶剂有水、乙醇、异丙醇、苯、甲醇、乙酸乙酯等几种,最常用的是水。
NVP在水和有机溶剂中的聚合机理是不同,在水溶液中的聚合机理如图1.3(以过氧化氢为引发剂)[16,17]:
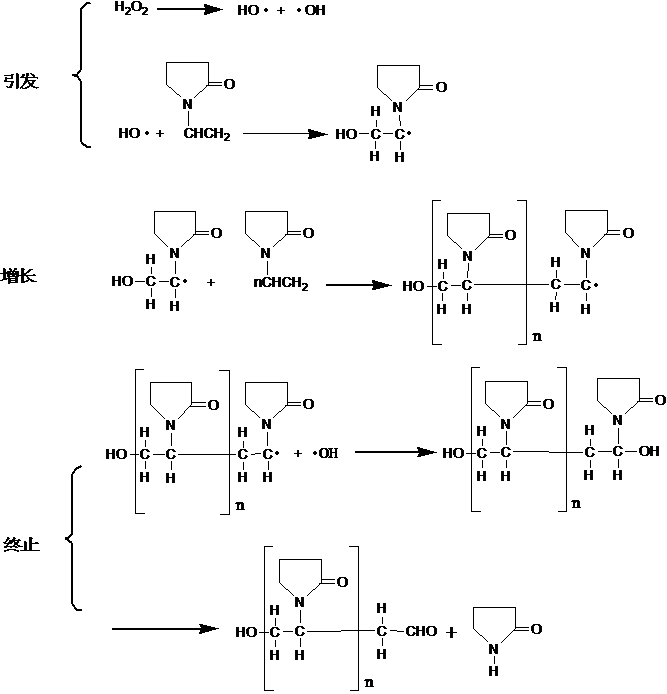
图1.3 NVP在水中的聚合机理
NVP在水溶液进行聚合时,长链自由基通常是和引发剂自由基结合而终止的,而且在链终止阶段,会同时发生吡咯烷酮环的裂解反应,因此经常发现醛基是PVP的一种端基。裂解反应也会有少量的吡咯烷酮生成,所以水溶液聚合得到的聚合物不是特别纯。
由于水溶液聚合中,长链自由基是通过与引发剂自由基结合而终止的,所以引发剂的量对聚合物分子量的影响特别大[18]。
动力学链长是增长反应速度和终止反应速度的比值:
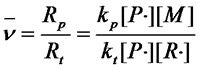 (式1.1)
(式1.1)

而
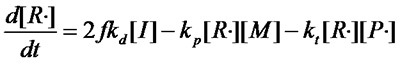 (式1.2)
(式1.2)
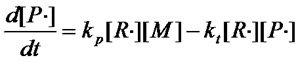 (式1.3)
(式1.3)
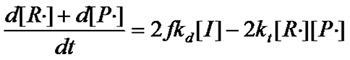 (式1.4)
(式1.4)
根据稳态假设,聚合体系中的自由基浓度保持不变,所以
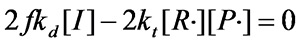 (式1.5)
(式1.5)
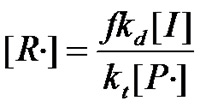 (式1.6)
(式1.6)
将式1.6代入式1.1,得到:
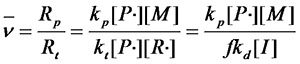 (式1.7)
(式1.7)
式1.7与通常的双基终止方式的动力学链长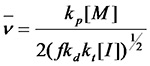 相比,引发剂浓度对分子量的影响要大多了。
相比,引发剂浓度对分子量的影响要大多了。
而且NVP和水还有氢键作用,这对其反应活性也有影响。图1.4是初始反应速度与NVP在水中浓度的关系[19]。

图1.4 氢键对NVP聚合反应速度的影响
从图中可以看出,在NVP浓度为75%(vol)时,对应的NVP和水的摩尔比为1:2,聚合反应速度最大,而且此时的体系粘度也是最高。这种氢键作用可以提高NVP的反应活性,从而提高了反应速度。而过量的水又稀释了NVP-水的氢键结合物,导致NVP浓度低时,反应速度也下降。
NVP在醇类等有机溶剂中进行聚合反应时,反应机理比较复杂,如图1.5所示。
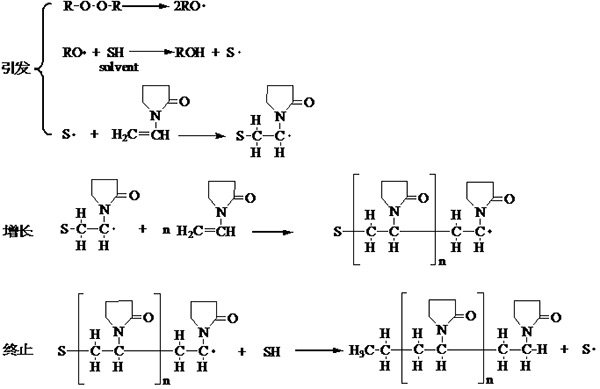
图1.5 NVP在有机溶剂中的聚合机理
在有机溶剂中进行聚合时,引发单体聚合的是引发剂自由基与溶剂反应生成的溶剂自由基,链的终止是通过向溶剂链转移完成的,得到一个氢原子的端基和另一个溶剂自由基,继续引发聚合反应。由于终止反应中没有像在水溶液中聚合那样,发生吡咯烷酮环的裂解,因此制备的聚合物较纯;没有醛基端基存在,在氧化条件下也比水溶液聚合更稳定。但由于链转移反应,在有机溶剂中聚合一般只能得到较低分子量的聚合物,如果要合成高分子量的聚合物,就必须要在水溶液中,使用小剂量的引发剂。
2.共聚
NVP除了可以均聚外,还可以与其他含有乙烯基结构的单体发生共聚反应,生成各种不同性能的共聚物。
可以与NVP发生共聚反应的单体如表1.2所列。
表1.2 可以与NVP发生共聚反应的单体 | |
酯类 | 二甲基氨基乙基甲酸丙烯酯、乙酸丙烯酯、异丁烯酸酯、二乙酸丙烯酸酯、甲基丙烯酸甲酯、乙酸乙烯酯、二碳酸乙烯酯、丙酸乙烯酯、丙烯酸异丙烯酯、三烯丙基异腈尿酸酯、二甲胺乙烯异丁烯酸酯、二甲胺乙烯甲基丙烯酸甲酯、乙烯基丙烯酸酯、三丁基丙烯酸酯、丙烯酸异辛酯等 |
醚类 | 乙烯基苯基醚、乙烯基异丙基醚、乙烯基环己基醚、乙烯基丁基醚等 |
烃类 | 乙烯、苯乙烯、十六碳烯 |
酰胺类 | N-乙烯基苯亚酰胺、丙烯酰胺、乙烯基己内酰胺 |
卤代烃类 | 氯乙烯、三氯乙烯 |
醇类 | 丙烯醇 |
双官能团类(交联聚合) | 亚甲基双丙烯酰胺、二乙烯基苯 |
其他类 | 丙烯腈、马来酸酐、乙烯基三甲基硅烷、乙烯基三甲氧基硅烷、乙烯基咪唑等 |
虽然自由基聚合可以得到很多NVP的共聚物,但是目前只有少数几种有大量的工业生产,如NVP/醋酸乙烯酯、NVP/丙酸乙烯酯,主要应用在化妆品、印染助剂和食品添加剂。
表1.3 一些不饱和单体对NVP(M1)的共聚参数[20] | ||||
单体(M2) | r1 | r 2 | Q | e |
二碳酸乙烯酯 | 0.4 | 0.7 | — | — |
月桂酸乙烯酯 | 1.15~1.3 | 0.01 | — | — |
乙酸乙烯酯 | 2.0 | 0.24 | — | — |
甲基丙烯酸甲酯 | 0.005 | 4.7 | 0.074 | -1.33 |
二乙酸丙烯酯 | 0.92 | 0.94 | 0.096 | -1.27 |
乙酸丙烯酯 | 1.6 | 0.17 | — | — |
N-乙烯基苯亚酰胺 | 0.35 | 0.04 | 0.088 | 0.37 |
马来酸酐 | 0.16 | 0.08 | — | — |
丙烯醇 | 1.0 | 0 | — | — |
丙烯腈 | 0.06 | 0.18 | — | — |
苯乙烯 | 0.045 | 15.7 | 0.087 | -1.22 |
三氯乙烯 | 0.54 | <0.01 | — | — |
氯乙烯 | 0.38 | 0.53 | 0.035 | -1.07 |
乙烯基苯基醚 | 4.43 | 0.22 | — | — |
乙烯基异丙基醚 | 1.68 | — | — | — |
乙烯基环己基醚 | 3.84 | — | — | — |
乙烯基丁基醚 | 3.30 | 0.205 | 0.067 | -1.12 |
3.交联聚合
NVP的线性聚合物PVP是一种水溶性高分子,但是其交联聚合物就不能溶于水和有机溶剂了。
有三种方法可以合成得到交联的PVP:
a)用过硫酸盐、肼或者过氧化氢处理PVP,或者在过氧化物存在下,用α,ω-二烯烃处理PVP,都可以得到低交联度的PVPP,生成的产物为软凝胶[21-23] 。
b)添加交联剂的自由基聚合[24]。常用的交联剂有:二乙烯基苯、N,N’-亚甲基双丙烯酰胺、二甲基丙烯酸乙烯酯、α,ω-二烯烃等。采用这种方法合成PVPP时,可以通过控制交联剂的用量来控制PVPP的交联程度。但这种方法也只能得到中等交联度的PVPP,如果要得到很高交联度的PVPP,需要加入很多量的交联剂,这样在工业上并不合算。
c)爆米花聚合[25-28]。采用这种方法合成得到的是高度交联的PVPP。
1.1.4 PVP的性质[29]
PVP是一种水溶性高分子化合物,具有水溶性高分子化合物的一般性质,如胶体保护作用、成膜性、粘接性、吸湿性、增溶或凝聚作用、与某些化合物的络合能力等。但PVP最具特色的是它的优良的溶解性能和生理惰性。PVP既溶于水,又溶于大部分有机溶剂,无毒无害,生理相容性很好。
1.分子量的测定及其表征
商品PVP按分子量大小分成若干等级,一般用Fikentscher法的K值来表示。测定K值最常用的方法是用毛细管粘度计测得PVP水溶液的相对粘度η,则有
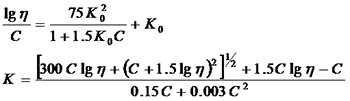
式中: K0 Fikentscher常数 K=1000 K0;
C 100ml溶解PVP的克数;
η 相对粘度
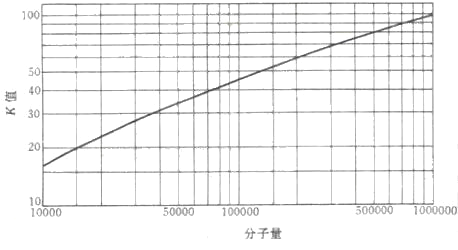
图1.6 PVP的K值和分子量的对应关系
2.物理性质
PVP在水中的熔解热为-4.8kJ/mol,折射率 。PVP的固体密度为1.25×103kg/m3,但由于结构疏松,其堆密度随分子量和干燥方法的不同,在0.1~0.6g/ml范围内。
PVP的玻璃化温度也随分子量的增加而升高,其极限值约为180℃,如图1.7所示:
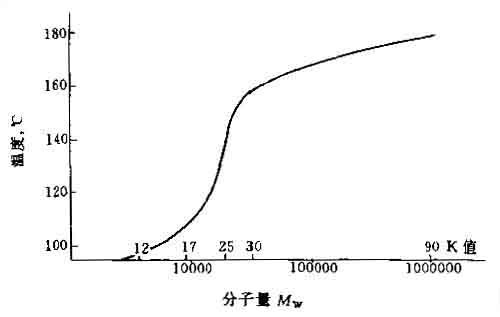
图1.7 PVP的玻璃化温度
PVP的X-射线散射角2θ分别为10°~26°和10°~40°,这表明PVP是无定型非晶态结构。
3.溶解性和溶液特性
由于PVP分子中既有亲水基团,又有亲油基团,所以可以与许多溶剂相互作用,使其既能溶于水,又能溶解于许多醇、羧酸、胺、卤代烃等有机溶剂中。PVP在水中的溶解度仅受它自身粘度的限制。
在室温下能溶解超过10%以上PVP的有机溶剂举例如表1.4,在室温下溶解PVP不超过1%的有机溶剂举例如表1.5。
从表1.4和表1.5可以看出,PVP一般易溶于有较强极性的溶剂,而不易溶于较弱极性的溶剂,但当有助溶剂存在时,则可溶于烃类等非极性溶剂。
表1.4 容易溶解PVP的有机溶剂 | |
醇类 | 甲醇、乙醇、丙醇、异丙醇、丁醇、异丁醇、戊醇、环己醇、甲基环己醇、苯酚、乙二醇、丙二醇、丁二醇、甘油、二丙酮醇 |
酸类 | 甲酸、乙酸、丙酸 |
内酯类 | γ-丁内酯 |
醚-醇类 | 乙二醇醚、二甘醇、三甘醇、1,6-己二醇、聚乙二醇400、2,2’硫代二乙醇 |
酯类 | 乳酸乙酯 |
酮类 | 甲基环己酮、环己酮(热) |
内酰胺类 | 2-吡咯烷酮、N-甲基吡咯烷酮、N-乙烯基吡咯烷酮 |
胺类 | 丁胺、环己胺、苯胺、乙二胺、吡啶、吗啉、乙醇胺、二乙醇胺、三乙醇胺、氨乙基乙醇胺、2-羟基乙基吗啉、2-氨基-2-甲基丙醇 |
硝基烃类 | 硝基甲烷、硝基乙烷 |
表1.5 不易溶解PVP的有机溶剂 | |
烃类 | 苯、甲苯、二甲苯、石油醚、四氢萘、戊烷、己烷、庚烷、干洗溶剂油、煤油、溶剂油、矿物油、环己烷、甲基环己烷、松节油 |
醚类 | 二氧六烷、二乙醚、二甲醚、乙基乙烯基醚、异丁基乙烯基醚、四氢呋喃 |
含氯类 | 四氯化碳、氯苯 |
酮类 | 丙酮、2-丁酮、环己酮 |
酯类 | 醋酸乙酯、醋酸异丁酯 |
在较大的范围里,PVP水溶液的粘度与pH值无关,仅仅在极限的情况下会有较大变化:浓盐酸会增加溶液的粘度,浓碱会使PVP发生沉淀。
PVP在其他有机溶剂中的粘度变化较大,如表1.6所示。对于有些有机溶剂,溶液粘度增大的原因是由于PVP在与其混合后,引起凝胶化作用所致。
表1.6 在不同溶剂中10%PVP K30溶液粘度,25℃ | |||||||
溶剂 | 二氯甲烷 | N-甲基吡咯烷酮 | 水 | 乙醚 | 丙二醇 | 乙二醇 | 异丙醇 |
粘度,mm2/s | 3 | 8 | 5 | 12 | 261 | 95 | 12 |
溶剂 | 二乙二醇 | 三乙醇铵 | 乙醇 | 醋酸 | 环己醇 | 丙三醇 | 丁二醇 |
粘度,mm2/s | 165 | 666 | 5 | 12 | 376 | 2046 | 425 |
将PVP溶解在NaCl水溶液里(0.2mol或2mol),其行为特征如粘度等与PVP水溶液仅有细微差别,这是PVP区别与其他大多数聚合物的优异特性。
PVP在混合溶剂中溶解性也有比较特别的地方。如PVP/丙酮/水的三元体系,其相图如图1.9所示。从相图可知,由于丙酮对PVP几乎不溶,所以当在PVP的水溶液中加入大量的丙酮,则部分PVP会随丙酮沉淀,形成两相。三相共溶点的位置随K值的减小而趋向丙酮比例增大的方向。
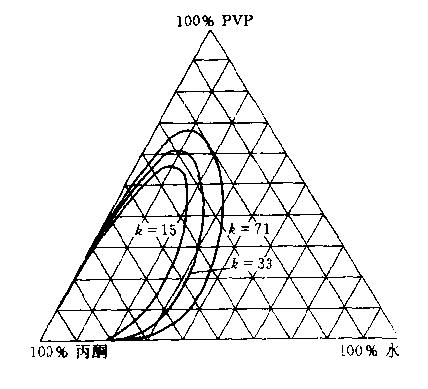
图1.9 PVP/丙酮/水的三元体系相图(25℃)
4.表面活性
从结构看,PVP长分子链中既有亲水和亲合极性基团的内酰胺基,又有亲油性的非极性的碳链,PVP的这种分子结构使其带有表面活性。其降低表面或界面张力的能力虽然比低分子表面活性剂小,渗透能力也较弱,但其对固体表面的吸附作用及亲水性所形成的立体屏蔽能力,使固体粒子具有优良的分散稳定性。此外他与许多有机无机化合物的氢键络合能力又使其具有凝聚作用或增溶能力,前者使其在含多酚类物质的酒类和饮料中起澄清和稳定作用,而后者则广泛应用于共沉淀制备药物固体分散体以提高难溶药物的生物利用度。以上这些表面活性物质的综合特性使PVP成为高分子表面活性剂的主要品种之一。
5.吸湿性
PVP有较强的吸湿性,它在不同相对湿度下的饱和湿含量如图1.10。
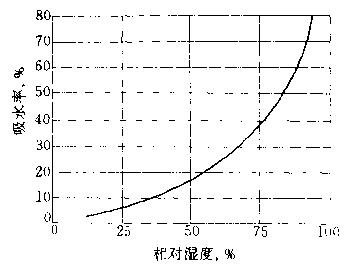
图1.10 PVP的饱和湿含量
热化学研究表明,每个NVP单元大约缔合0.5分子的水,这与蛋白质的吸水性相似。
6.络合性
PVP是一种具有高“溶解”能力的聚合物,这种“溶解”能力是因为其分子结构中有高极性特性和能接受氢键的酰胺基团,同时又有非极性基团。这种能力使得PVP能够与许多物质,特别是含羟基、羧基、氨基及其他活性氢原子的化合物生成络合物。
7.化学稳定性
通常情况下,固体PVP很稳定,在100℃空气中加热16小时无变化。PVP的水溶液在通常情况下也很稳定。不含其他成分时,0~100℃范围内PVP水溶液无任何沉淀迹象,但如果受热时间过长,或存放时间过长,或PH值在酸性范围内,都会使PVP溶液变成轻微的淡黄色。在PVP水溶液中加入各种含多价阴离子的盐类,如偏硅酸钠、三聚磷酸钠,PVP则会沉淀。但高分子量的PVP,无论是水溶液,还是干粉状态,存放时间过长都会有降解现象。
8.生物特性
PVP无毒,具有优良的生理惰性,不参与人体新陈代谢,它又具有优良的生物相容性,对皮肤、粘膜、眼等不形成任何刺激。
1.1.5 PVP的用途[30]
1.医药
PVP在出现后不久就作为血浆扩容剂,在二战中抢救了众多伤员。
如今,PVP和纤维素类衍生物、丙烯酸类化合物一起成为三大主要合成药物辅料,在全世界范围内得到广泛的应用。它可以作为片剂、颗粒剂的粘结剂、注射剂的助溶剂、稳定剂、液体制剂的分散剂、包衣成膜剂及色素分散剂、难溶药物的共沉淀剂及眼药的延效剂、润滑剂等。交联不溶型PVP还可以作为片剂的药物崩解剂。
PVP还有很多作为非辅料的应用,其中最常见的就是作为杀菌消毒剂使用的PVP-I。
2.化妆品
PVP在化妆品中有许多功能,主要是对乳液、悬浮液等分散体系的稳定及增粘作用,护发定型类产品中的成膜作用,凝胶类产品中的凝胶化作用,护肤类产品中的润滑、保湿,泡沫类产品的泡沫稳定作用,以及在各类化妆品配方中作为色素稳定剂,除臭、保香剂,温和剂等。
3.酿酒和饮料工业
PVP及不溶性PVP在酿酒、饮料工业中可以作为啤酒、果酒、果汁的澄清剂和稳定剂。PVP可以和这些酒类、饮料中的多酚类物质络合,从而除去这些会使酒类、饮料变浑浊的物质。
4.涂料、颜料工业
在涂料、颜料、油墨、高分子合成及加工等工业过程或工业产品中,PVP以其优良的溶解性、成膜性、生理惰性、表面活性和络合能力等综合特点,而得到广泛的应用。
5.粘结剂
PVP对玻璃、金属和塑料表面具有特别的粘结力;加上其亲水性、分散稳定性、无触变性、增稠性等特点,使它广泛用于各种粘结剂配方中,如固体胶水棒、压敏胶及再湿性胶等。
6.其他
除了以上叙述的PVP的一些用途外,PVP还在采油、造纸等其他方面应用。由于其优异性能,近年来不断发现PVP有许多新的应用;采用新的聚合技术和共聚方法,聚合物的性质能进一步改进,从而打开了一些全新的应用领域。